AMNOG einfach erklärt: Frühe Nutzenbewertung & Preisverhandlung | juravendis Glossar
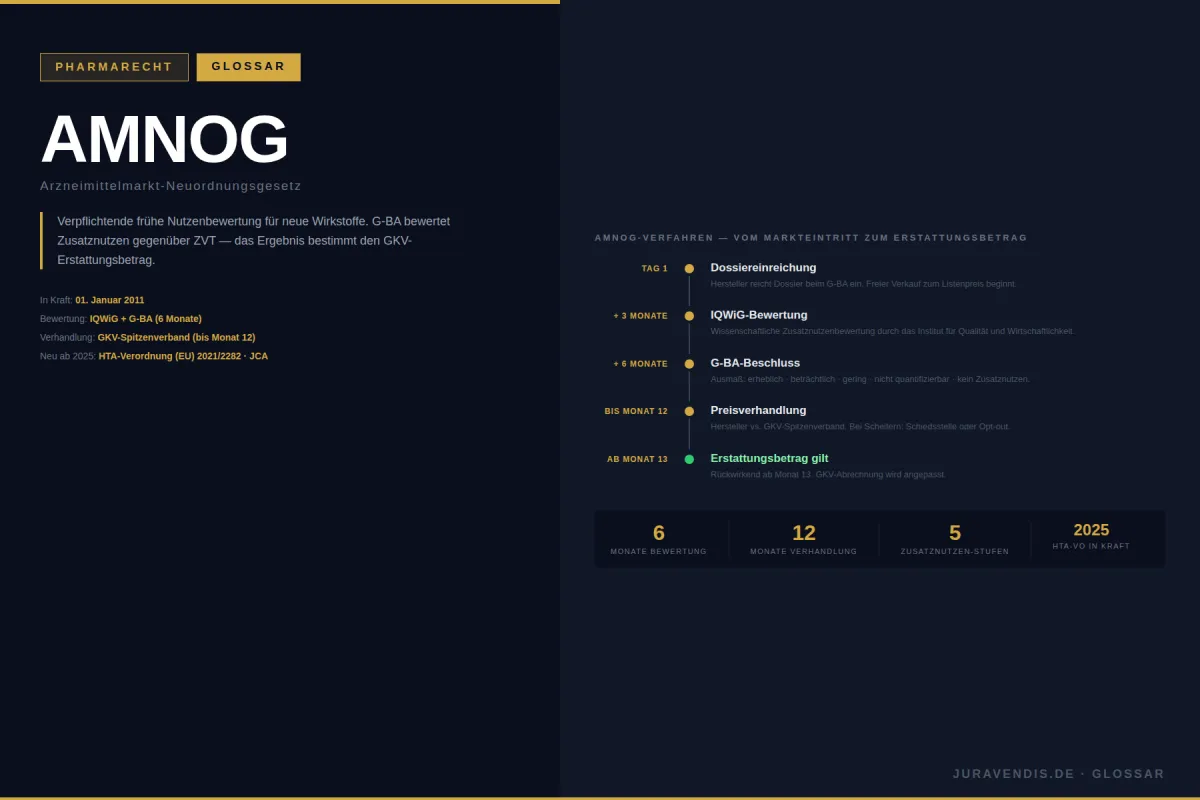
AMNOG: Verpflichtende frühe Nutzenbewertung für neue Wirkstoffe seit 2011. G-BA-Beschluss nach 6 Monaten, Erstattungsbetrag ab Monat 13. HTA-Verordnung (EU) 2021/2282 ergänzt das Verfahren ab Januar 2025 für Onkologika und ATMPs.
Benannte Stelle: Was sie prüft und warum der Engpass eskaliert | juravendis Glossar
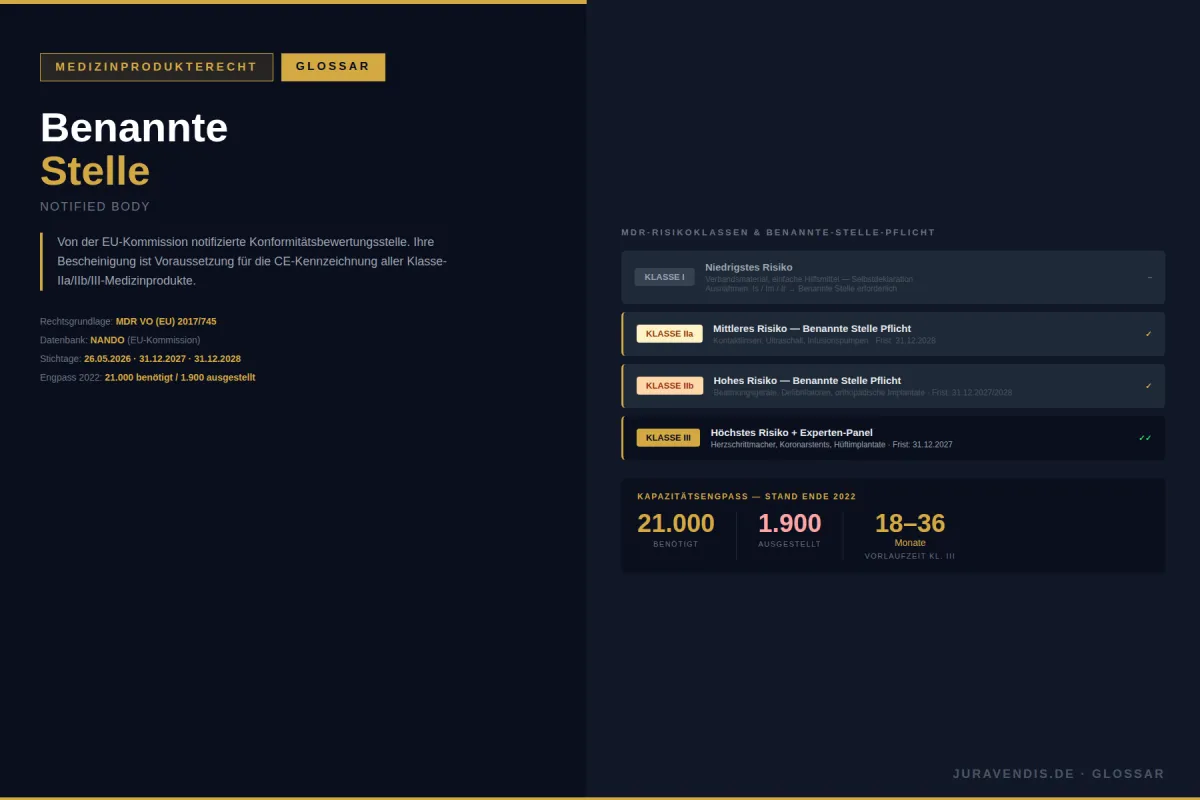
Benannte Stelle (Notified Body): Pflicht für CE-Kennzeichnung der Klassen IIa, IIb, III. Ende 2022: 21.000 benötigte vs. 1.900 ausgestellte MDR-Zertifikate. Übergangsfristen bis 2027/2028. Vorlaufzeit Klasse III: 18–36 Monate.
Novel Food: Was ist das? EU-Verordnung, Zulassung & Praxis | juravendis Glossar
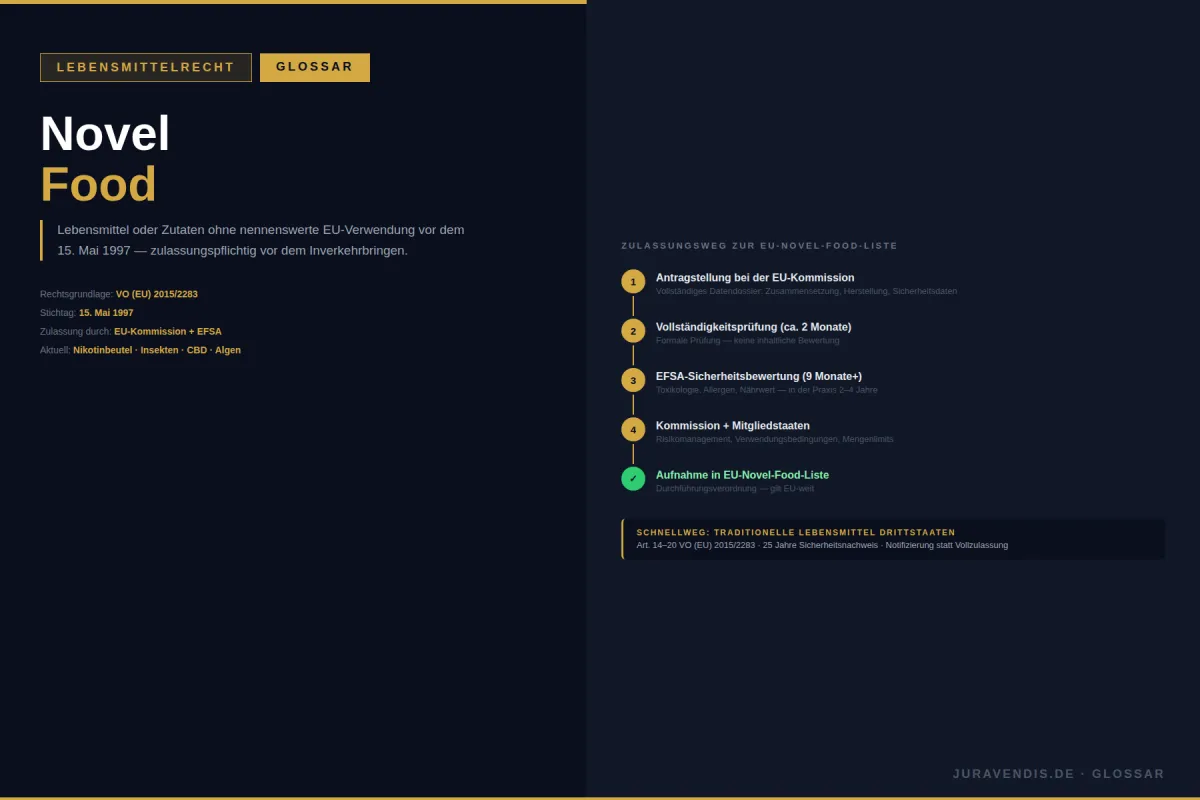
Novel Food = Lebensmittel ohne nennenswerte EU-Verwendung vor dem 15.05.1997. VO (EU) 2015/2283: Zulassung via EFSA erforderlich. Nikotinbeutel als Novel Food in Deutschland: gewerblicher Verkauf verboten. Insekten: 4 Arten zugelassen.
CPNP: Das EU-Kosmetik-Notifizierungsportal erklärt | juravendis Glossar
Das CPNP ist das EU-Pflichtportal für die Notifizierung kosmetischer Mittel (Art. 13 VO (EG) 1223/2009). 8 Pflichtangaben, Verantwortliche Person, Giftnotrufzentrale. PFAS-Verbot Oktober 2026 erzwingt Neu-Notifizierungen.